Anvisa autoriza importação excepcional da vacina Sputnik V em mais 7 estados
A autorização foi concedida com as mesmas restrições que se aplicaram a outros 6 estados, incluindo a Bahia
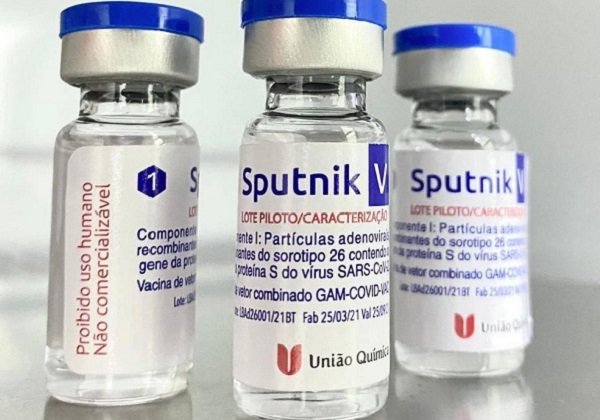
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou a importação excepcional da Sputnik V por mais 7 estados brasileiros: Rio Grande do Norte, Mato Grosso, Rondônia, Pará, Amapá, Paraíba e Goiás.
Ao todo, mais 592 mil doses poderão ser importadas, distribuídas da seguinte forma:
Rio Grande do Norte: 71 mil
Mato Grosso: 71 mil
Rondônia: 36 mil
Pará: 174 mil
Amapá: 17 mil
Paraíba: 81 mil
Goiás: 142 mil
A autorização foi concedida com as mesmas restrições que se aplicaram a outros 6 estados que também receberam, no início do mês, permissão de importação excepcional – Bahia, Maranhão, Sergipe, Ceará, Pernambuco e Piauí. Ao todo, esses estados tiveram autorização para importar 928 mil doses.
Condições:
Entre algumas das condições estão:
A vacina deverá ser utilizada apenas em adultos saudáveis.
Todos os lotes importados só poderão ser usados após liberação pelo Instituto Nacional de Controle de Qualidade em Saúde da Fiocruz.
A Anvisa receberá relatórios periódicos de avaliação de risco-benefício da vacina.
A vacina deverá ser utilizada em condições controladas, com condução de estudo de efetividade, com delineamento acordado com a Anvisa e executado conforme boas práticas clínicas.
A Anvisa poderá, a qualquer momento, suspender a importação, distribuição e uso das vacinas importadas.
As pessoas deverão ser informadas de que a vacina “não tem avaliação” da agência quanto a qualidade, eficácia e segurança.
A vacina NÃO poderá ser aplicada nos seguintes casos:
Pessoas com hipersensibilidade a qualquer dos componentes da fórmula
Gravidez; lactantes; menores de 18 anos ou maiores de 60 anos;
Mulheres em idade fértil que desejem engravidar nos próximos 12 meses;
Enfermidades graves ou não controladas e antecedentes de anafilaxia
Pessoas que tenham recebido outra vacina contra a Covid-19; pessoas com febre, vivendo com HIV, hepatite B ou C, pessoas que tenham se vacinado nas 4 semanas anteriores e que tenham recebido imunoglobulinas ou hemoderivados 3 meses antes.
Pessoas que tenham recebido tratamentos com imunossupressores, citotóxicos, quimioterapia ou radiação 36 meses, tenham recebido terapias com biológicos incluindo anticorpos anticitocinas e outros anticorpos.
A Anvisa frisou ainda que todos os lotes dos imunizantes importados somente poderão ser destinados ao uso após liberação pelo Instituto Nacional de Controle de Qualidade em Saúde (INCQS).
Além disso, a Anvisa receberá relatórios periódicos de avaliação benefício-risco da vacina; o imunizante deverá ser utilizado em condições controladas com condução de estudo de efetividade, com delineamento acordado com a Agência e executado conforme Boas Práticas Clínicas; a Anvisa poderá, a qualquer momento, suspender a importação, distribuição e uso das vacinas importadas; dentre outros aspectos destacados no voto do relator.
 Covid-19 Brasil registra 11.722 casos de covid-19 e 92 mortes em 24 horas
Covid-19 Brasil registra 11.722 casos de covid-19 e 92 mortes em 24 horas  Covid-19 Bahia registra 567 novos casos e mais 11 óbitos nesta terça-feira (30)
Covid-19 Bahia registra 567 novos casos e mais 11 óbitos nesta terça-feira (30) 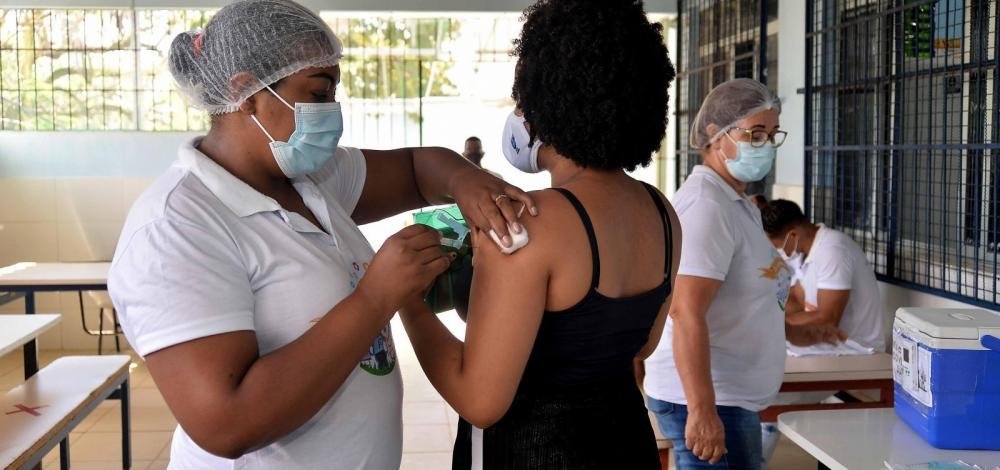 Confira! Covid-19: Saiba onde se vacinar em Salvador nesta quarta
Confira! Covid-19: Saiba onde se vacinar em Salvador nesta quarta  Salvador Salvador segue com aplicação das doses contra Covid-19 nesta sexta
Salvador Salvador segue com aplicação das doses contra Covid-19 nesta sexta  Salvador Covid-19: prefeitura retoma vacinação em Salvador nesta segunda-feira (8)
Salvador Covid-19: prefeitura retoma vacinação em Salvador nesta segunda-feira (8)  Confira! Covid-19: Confira os postos de vacinação em Salvador nesta terça
Confira! Covid-19: Confira os postos de vacinação em Salvador nesta terça 








